Posts tagged ‘ANVISA’
ブラジル国家衛生監督局(ANVISA)による事前承認制度の廃止
長い間にブラジル特許制度の特徴的な課題となったブラジル国家衛生監督局(ANVISA)による事前承認制度は改正法により廃止されました。今回の改正法案は、2021年3月に公布された暫定措置令(MP[i])1040/21(MP1040/21)に基づく法案であり、 開業促進などのビジネス環境の改善を主な目的とするものでした。この暫定措置令1040/21には、医薬特許付与の要件として、ブラジル国家衛生監督局(ANVISA)による事前承認制度を規定しているブラジル産業財産法第229-C条の廃止も含まれていました。なお、議会において暫定措置令1040/21の立法化について検討された際に一部修正されたため、転換法案15/2021(PLV 15/2021)となりました。
ブラジル産業財産法第229-C条に規定されているブラジル国家衛生監督局(ANVISA)による事前承認制度とは、ブラジル特許庁(INPI)に出願された医薬品関連の特許出願の場合、ANVISAによる事前承認手続きのためにANVISAに送付され、ANVISAが公衆衛生への影響について審査し、事前承認の審査後、ブラジル特許庁に再び送付される制度であす。事前承認が受けた場合、ブラジル特許庁において特許要件に関する実体審査が行われます。一方、事前承認を受けられなかった場合、ブラジル特許庁は事前承認を受けていないことを理由として出願を拒絶します。当該制度は2001年のブラジル産業財産法の改正により導入され、製薬会社の大きな負担となっていました。
2021年6月23日に下院議会において暫定措置令1040/21が承認され、法案に転換されました。その後、8月4日、上院議会が同法案を可決したものの、法案の一部が改訂されたため、改めて下院議会に送付されました。8月5日、下院議会は、上院議会が提案した改訂案を却下し、8月6日にボルソナロ大統領による裁可のために送付されました。その後、ボルソナル大統領が同法案を裁可し、8月26日に第229-C条の廃止を定めた第57条を含む、法律14.195/21が成立しました。同法律により、医薬品関連の特許出願の際のブラジル国家衛生監督局(ANVISA)による事前承認制度が廃止されることとなりました。

ブラジル特許庁は、8月31日に交付した公報[ii]において、法律14,195/2021による第229-C条の廃止に伴う医薬品関連の特許出願に関する手続きを公表しました。その内容は以下の通りです。
- 2021年8月27日以降、ブラジル特許庁はANVISAに医薬品関連特許出願を転送していない。
- ANVISAから返却された出願については、第229-C条が廃止されたことを示す通知コード7.7が交付され、その後、通常の審査手続きに戻る。
- 第229-C条の廃止前にANVISAによる事前承認の手続きが完了していた出願は、8月23日にブラジル特許庁に転送され、当該出願について従来通りに事前承認(通知コード7.5)または事前承認拒否(通知コード7.7)の通知コードが交付される。
- 2016年12月31日までに行われた出願で、バックログ解消計画に含まれている出願は、通常通りに「Preliminary Office Action」に関する通知コードの6.21または6.22が交付される。
しかしながら、ANVISAにおいて事前承認手続き待ちとなっていた出願の全てがブラジル特許庁において審査が行われようになるまでには少し時間かかるものの、この改正は製薬業界にとって大変ポジティブな情報といえます。日本企業に関しては、ANVISAにおよそ70件程度の出願が残っていたが、近いうちにブラジルの事前承認制度から逃れることができるようになります。
ご質問がありましたら、お気軽にご連絡ください。
[i] 暫定措置令(MP)とは、緊急性のある場合に限り、大統領が独自に発令できるものであり、法律と同様の拘束力を有します。なお、暫定措置令は、大統領による発令後、議会において立法化に関する検討が行われなければならない。
[ii] https://www.gov.br/inpi/pt-br/central-de-conteudo/noticias/inpi-divulga-procedimentos-apos-extincao-da-anuencia-previa-de-patentes-farmaceuticas
ブラジル特許庁は意匠の電子出願を開始する
計画から長い時間が経ったが、ブラジル特許庁(INPI)は2015年4月22日より電子出願システムを開始し、意匠電子出願を受理することが発表された。意匠電子出願制度は決議146/2015に基づいて制定され、当決議は2015年4月7日の公報に公開された。
意匠電子出願はブラジル特許庁の電子化における最新のステップである。ブラジル特許庁は最初2006年に商標のための「e-Marcas」を始め、当商標電子出願制度が2011年に更新された。2011年には、INPIが「e-Patentes」のパイロットを開始したが、そ の特許のためのシステムの本格的なバージョンは2013年に公開され、実施されてきた。2014年、ブラジル特許庁は特許、実用新案、意匠および商標の調査のツールの更新を行った。
の特許のためのシステムの本格的なバージョンは2013年に公開され、実施されてきた。2014年、ブラジル特許庁は特許、実用新案、意匠および商標の調査のツールの更新を行った。
ブラジル特許庁において審査を早くするため、かつバックログ解決方法を目的としてINPIは電子化活動に力を入れているわけである。ブラジル特許庁の電子化プロジェクトによって、出願人は電子に出願することが可能になることのみならず、一部のケースに関する意見書、拒絶通知書、先行技術、異議申立等に電子的にアクセスが可能になった。
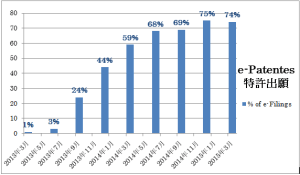
 ブラジル特許庁のサイトではブラジルにおける電子出願の使用について面白い統計が入っており、現在、およそ74%の出願が電子的に提出されているようである。
ブラジル特許庁のサイトではブラジルにおける電子出願の使用について面白い統計が入っており、現在、およそ74%の出願が電子的に提出されているようである。
 ブラジルで意匠は、特許および商標と異なり、無審査主義を採っている。従って、意匠電子出願システムの制定によってブラジル特許庁は意匠に関するバックログを本格的に減少させる見通しである。現在、ブラジル特許庁は意匠の登録を発行するまでに平均6カ月がかかる。当電子出願システムが正常に実施された場合、この時間を大幅に減少させることが可能であろう。
ブラジルで意匠は、特許および商標と異なり、無審査主義を採っている。従って、意匠電子出願システムの制定によってブラジル特許庁は意匠に関するバックログを本格的に減少させる見通しである。現在、ブラジル特許庁は意匠の登録を発行するまでに平均6カ月がかかる。当電子出願システムが正常に実施された場合、この時間を大幅に減少させることが可能であろう。
ソース:「e-Trademarkに関する統計」、「e-Patentに関する統計」および「Resolução nº 146/2015」
ブラジルでの医薬品特許に関する新たな動き
2013年4月15日にANVISA(ブラジル国家衛生監督局)が医薬品に関する特許付与に関する事前承認について従来よりも承認審査の範囲が明確に理解できるように決議が発行された(2013年4月10日付RDC第21号決議)。2013年4月10日付RDC第21号決議の4条の規定によると事前承認については公衆衛生への影響について判断し、公衆衛生に反しない特許出願は承認を受けた後、特許要件の審査を行うためにINPIへ移送されることになる予定である。


ANVISA(ブラジル国家衛生監督局) Vs. INPI(ブラジル特許庁)
2013年4月10日付RDC第21号決議はポルトガル語の原文を読みたい方がここにアクセス下さい。Licks & Attorneysによる2013年4月10日付RDC第21号決議の英訳はここにアクセスできる。筆者による当該4条の条文の意訳は下記の様になる。
「4条 INPIに転送された特許出願を受理した後でANVISAが公衆衛生上の問題に照らしてそのような特許出願を審査し、当機関における適切な部門が発行する技術的な意見書に基づき査定される。
1項 下記の場合は特許出願が公衆衛生を違反しているとみなされる:
I号 特許出願に請求されている医薬品の製品及び方法は健康への危険が生じる場合、又は;
II号 医薬品の製品及び方法に関する特許出願は医薬品に関する政策又はSUS(Sistema Unico de Saude‐統一保健システム)における医薬援助について重要性があり、特許要件及びその他の1996年第9279号法律による要件が満たしていない場合。
2項 医薬品の製品及び方法ブラジルにおいて利用が禁止されることになった物体と関連されるときに健康への危険があるとみなされる。
3項 SUSのために保健省による戦略的な医薬品のリストを含めている省令又はその省令の改正に医薬品の製品及び方法が記載されている場合に、又は上記の省令に記載されている医療法と関連する医薬品の製品及び方法の場合に医薬品に関する政策又はSUSにおける医薬援助について重要性があるとみなされる。
4項 健康への危険あるいは医薬品に関する政策又はSUSにおける医薬救助について重要性を判断するための基準は他の法令等で規定が明確にされる。(…)」
最近開かれたANVISAの活動に関する公聴会において、ANVISA長官であるDirceu Barbano氏が上記の審査範囲について、事例を挙げて説明している「もしフェンプロポレックス(拒食症治療のための医薬品で、2012年に健康を害する恐れがあると判断され、医薬品製造業許可が取り消された)と似たような化学分子に関する特許が出願されれば、ANVISAが審査することになる。また、HAART療法のように公衆衛生に対して影響がある医療方法についても審査することになる。」
現在、保健省の戦略的医薬品リストについては978/2008省令書と改正1284/2010省令書によって定められている。当該リストに含めている事項はDi Blasi, Parente & Associatesによる英訳があり、ここにアクセスできる。
また、同様のリストはINPIによって2013年4月9日決議においても対象となっている。INPIによる決議No.80/2013を経て、INPIは医薬品に関する迅速に審査することの重要性を認め、医薬品及び医薬品の製造方法に関する特許出願に対して優先審査を請求できるようになった。優先審査は保健省又は出願人がSUSが定める戦略的医薬品リストに含まれている医薬品の製品及び製造方法に関する特許出願について、優先審査を請求することが可能になった。優先審査を請求するためには、対象となる特許出願が既に公開がされ、審査請求を提出する必要がある。優先審査請求が受理されてから1年以内に審査が行われる予定である。
同様の内容であるが、ANVISAの問題の歴史が含めている筆者による記事はNGB(日本技術貿易会社)のウェブサイトでアクセス下さい。
また、前にANVISA活動について、当サイトの記事はこちらになる。
ANVISAの事前承認の新たな流れ
早速ですが、2週間前のことであるが、とても大事な話なので提供する。
皆様のご存知の通りに、1999年12月14日改正法以降の医薬品に関する特許についてはANVISA(ブラジル国家衛生監督局)による事前承認を条件としている。
2012年5月25日までに、従来の事前承認の流れを簡単に説明すれば:
出願 → 公開 → 審査請求 → 特許査定* → ANVISAに移送 → ANVISAの審査
(*拒絶査定の場合にANVISAに送りませんでした)
という流れでしたが、ANVISAが出願を受けたときに、ブラジル特許庁が特許要件について査定(言い換えれば要件を満たしているということ)する旨の審決は既に包袋に入っている。それでANVISAが承認をし難くなると考えられた。なぜかというと何の根拠の下で拒絶するかといえば、技術的な理由ではなく、政治政策のような根拠になると思われた。
そして、2012年5月25日に、保健省(ANVISAの上部組織)と商務省(ブラジル特許庁の上部組織)が共同し法令1065号を発行した。
その法令には新たな流れを確定し、ANVISAもブラジル特許庁も管内にもそれに基づくガイドラインを発行する命令も含めている。
その新たな流れは以下のようになる。
出願 → 公開 → 審査請求 → 医薬品に関する出願であるか否かについて予備的な審査 → ANVISAに移送 → ANVISAの審査
新たな流れに関する問題が未だ明確について何も言えませんが、いくつかの問題を予測することがでる。
例えば、前にANVISAによる拒絶の理由が技術的な理由ではなく、政治政策のことでしたということを立証することできましたので、裁判にてANVISAによる拒絶はよりも取消請求が認めやすいと考えられた。


INPI(ブラジル特許庁) Vs. ANVISA(ブラジル国家衛生監督局)
ブラジル特許庁もANVISAも新たな流れを既に実施している(管内ガイドラインを発生しなくても)ということが確認できましたため、実務家は扱い方を変えないといけない。
これからに影響は本当に判断しづらいと思う。
流れが変わったといえどもANVISAによる審査の範囲の問題は恐らく狭くないといけないかもしれない。ただ、この新たな流れでANVISAが例え自分の審査の範囲を過ぎたとしたら、その立証がし難くなることは起きると考えられる。
また、動きがあったら、私が報告する。
カラペト・ホベルト